La Insuficiencia Cardiaca (IC) representa un síndrome clínico complejo que expresa la inhabilidad del corazón de realizar su función circulatoria con la eficiencia necesaria, condicionando la congestión característica y la aparición de síntomas.
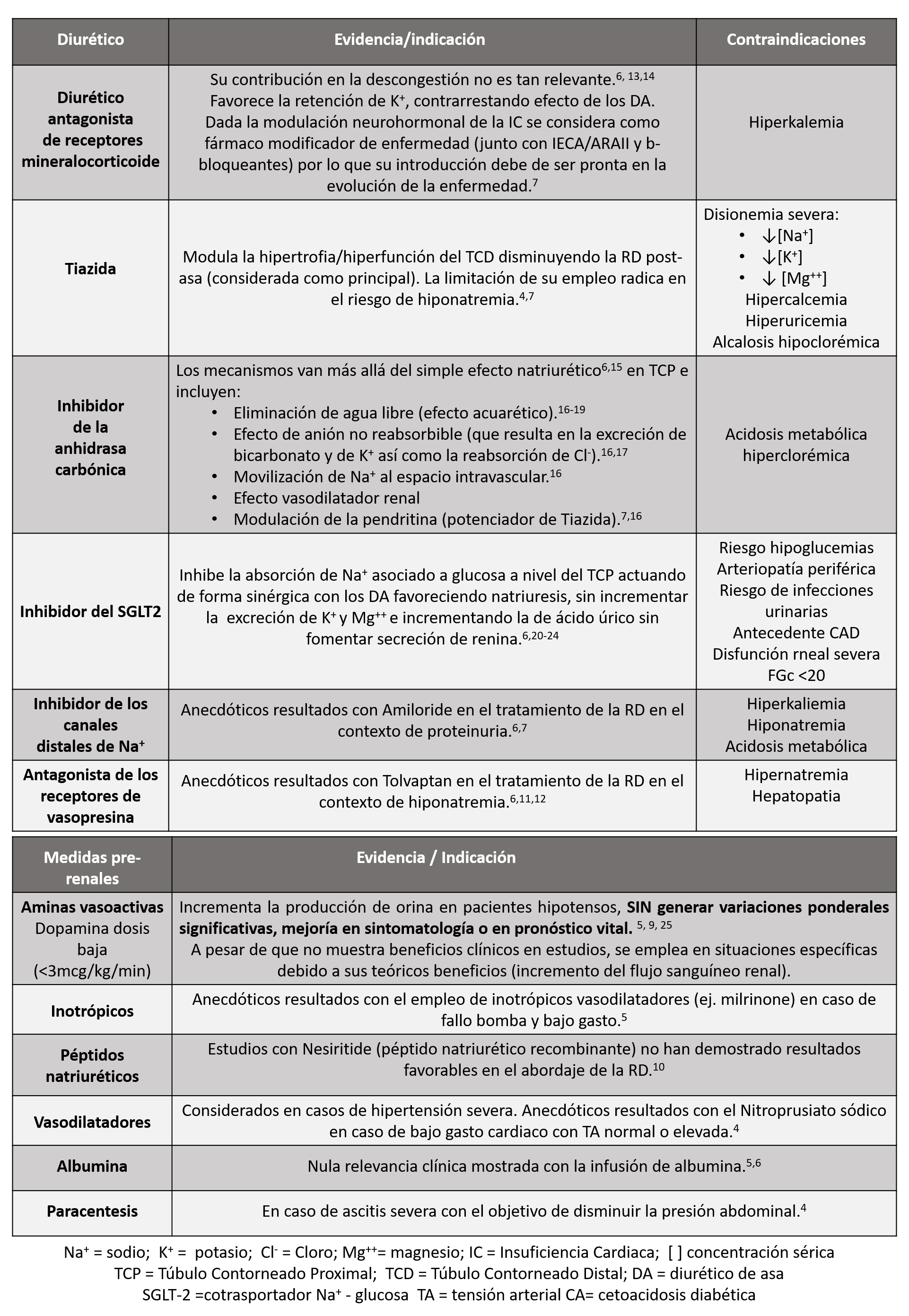
Su evolución se caracteriza por una curva de empeoramiento progresivo, de pendiente variable (en función de las características del paciente), con múltiples descompensaciones en contexto de procesos precipitantes (ej. infecciones, transgresiones dietéticas..) que conllevan a la depleción progresiva de reserva fisiológica hasta la aparición de refractariedad clínica y la muerte. No obstante, conforme avanza la enfermedad, la mayoría de dichas descompensaciones se corresponden más al empeoramiento de la función miocárdica consecuencia de la progresiva congestión que a la presencia de precipitantes agudos. 1 (ver imagen 1)
 Es por ello, que sin importar fracción de expulsión (conservada o reducida), los agentes diuréticos sean considerados como pilares fundamentales del tratamiento (siendo los de asa los principales representantes).2
Es por ello, que sin importar fracción de expulsión (conservada o reducida), los agentes diuréticos sean considerados como pilares fundamentales del tratamiento (siendo los de asa los principales representantes).2
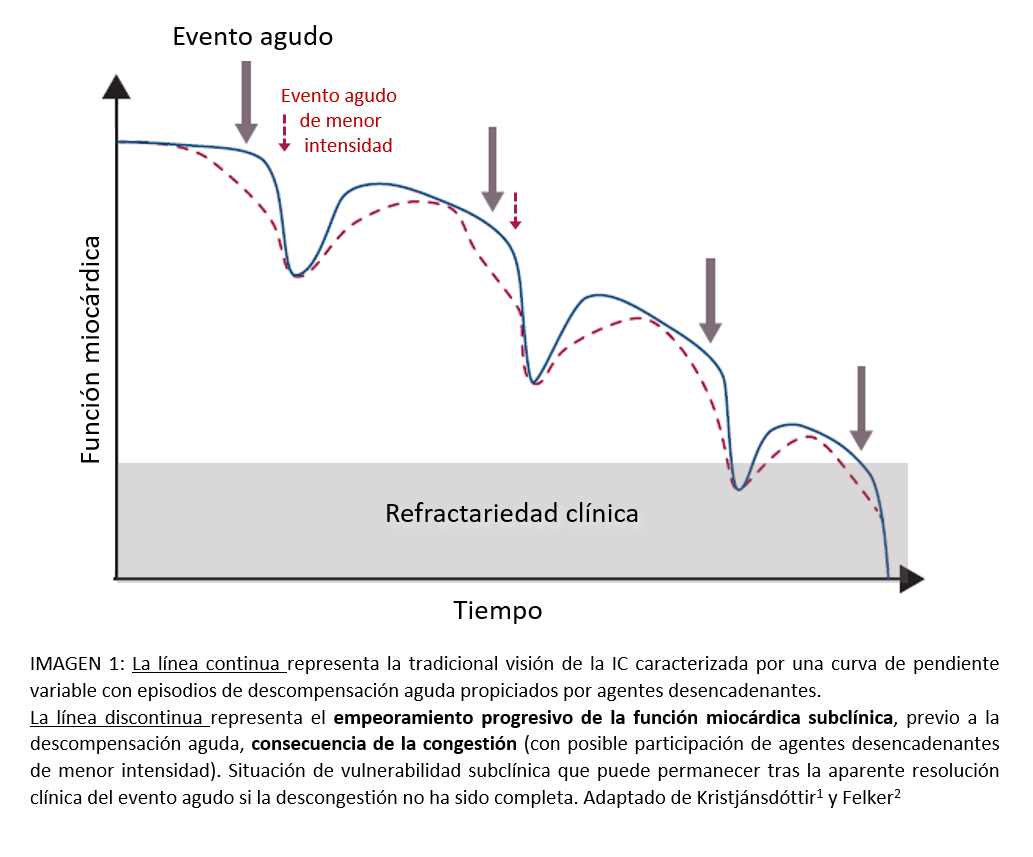
El empleo rutinario de dichos diuréticos, condicionado y agravado por la propia progresión de la enfermedad, incrementa de forma progresiva mecanismos fisiológicos compensadores que a la larga condicionan una pérdida de respuesta al diurético (a pesar de dosis adecuada), situación conocida como resistencia diurética.3 (ver imagen 2)
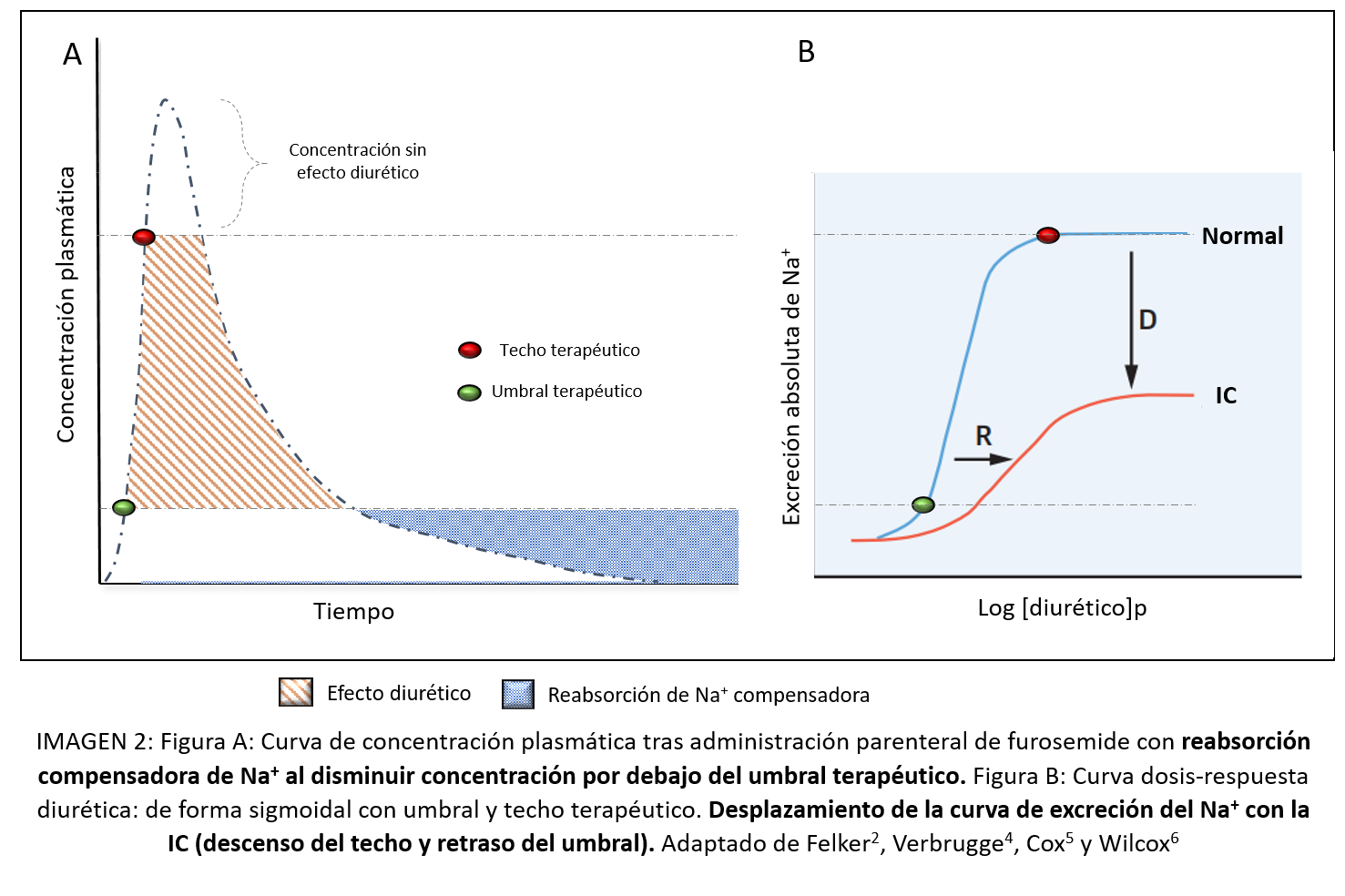

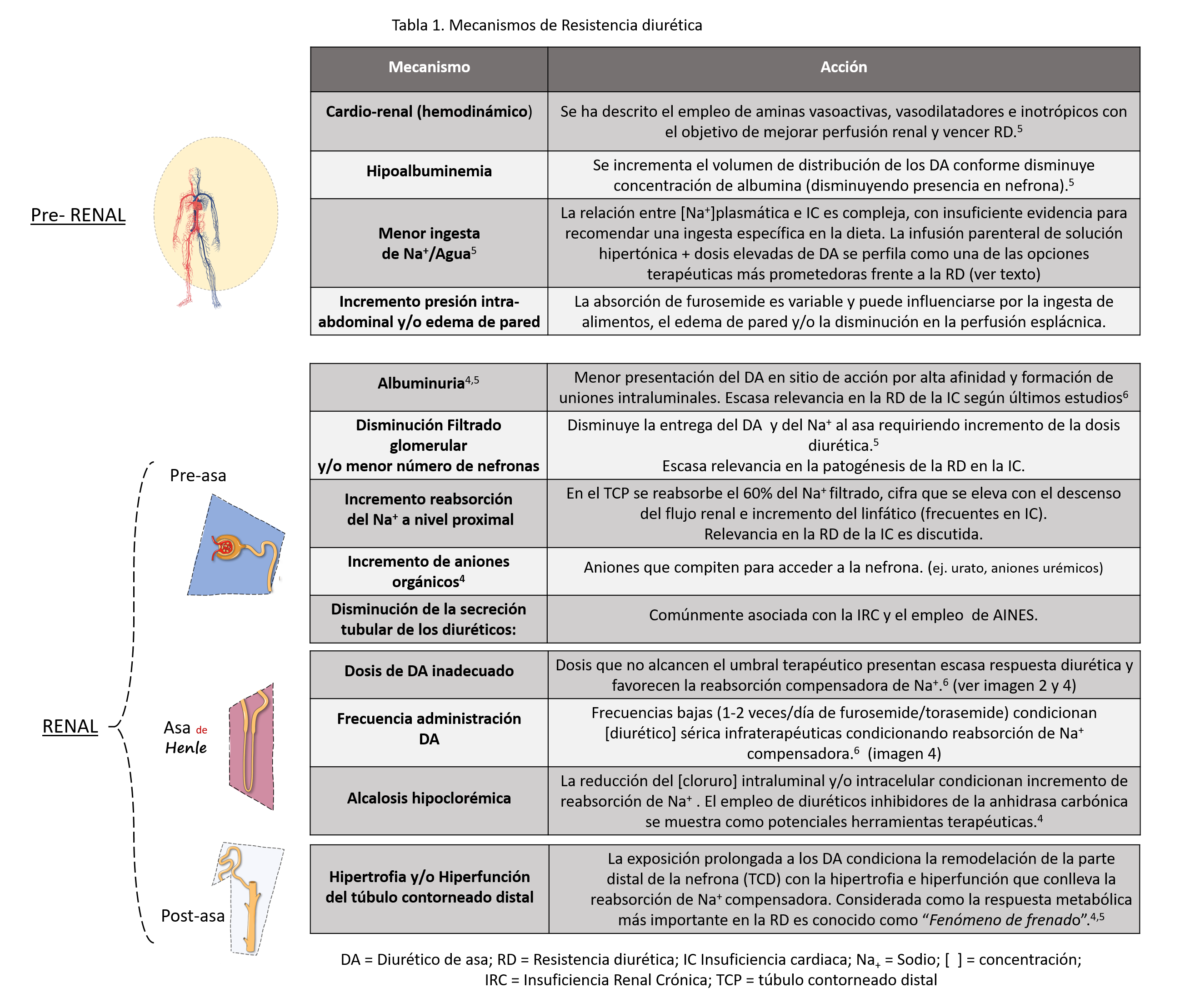
Diversos mecanismos se han asociado al desarrollo de dicha resistencia, mecanismos que van más allá del asa de Henle (sitio de acción de los diuréticos de asa) y que no suelen responder de forma mantenida al simple incremento de dosis, por lo que resulta necesario su conocimiento para así diseñar estrategias terapéuticas adecuadas.1-9
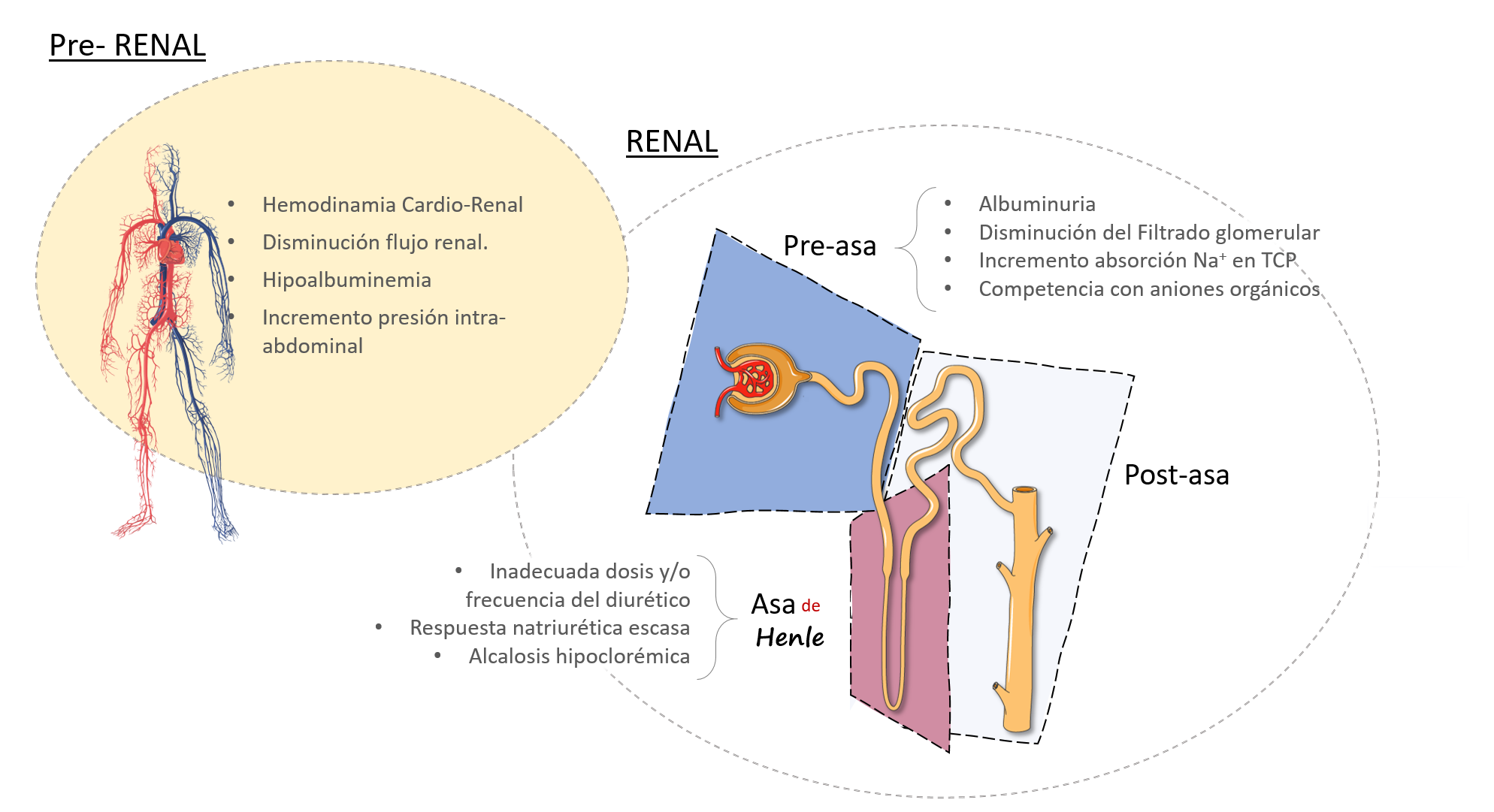
Imagen 3 clasificación de los diversos mecanismos que contribuyen a la RD
Los mecanismos de RD se clasifican en 2 grandes grupos: Pre-renal y Renal, siendo este último grupo subdividido en 3 en función de la relación con el asa de Henle.2-5 (Tabla 1)
ESTRATEGIAS TERAPEUTICAS CONTRA LA RESISTENCIA DIURETICA
El paso lógico inicial al objetivar un incremento del volumen extracelular (que no responde a una dosis establecida) podría considerarse en la modulación del propio DA con un incremento de dosis, de frecuencia, cambio de vía de administración (ver imagen 4A) o rotación del diurético por otro de su misma familia con mejores propiedades farmacocinéticas (ej. furosemide -> torasemide).2
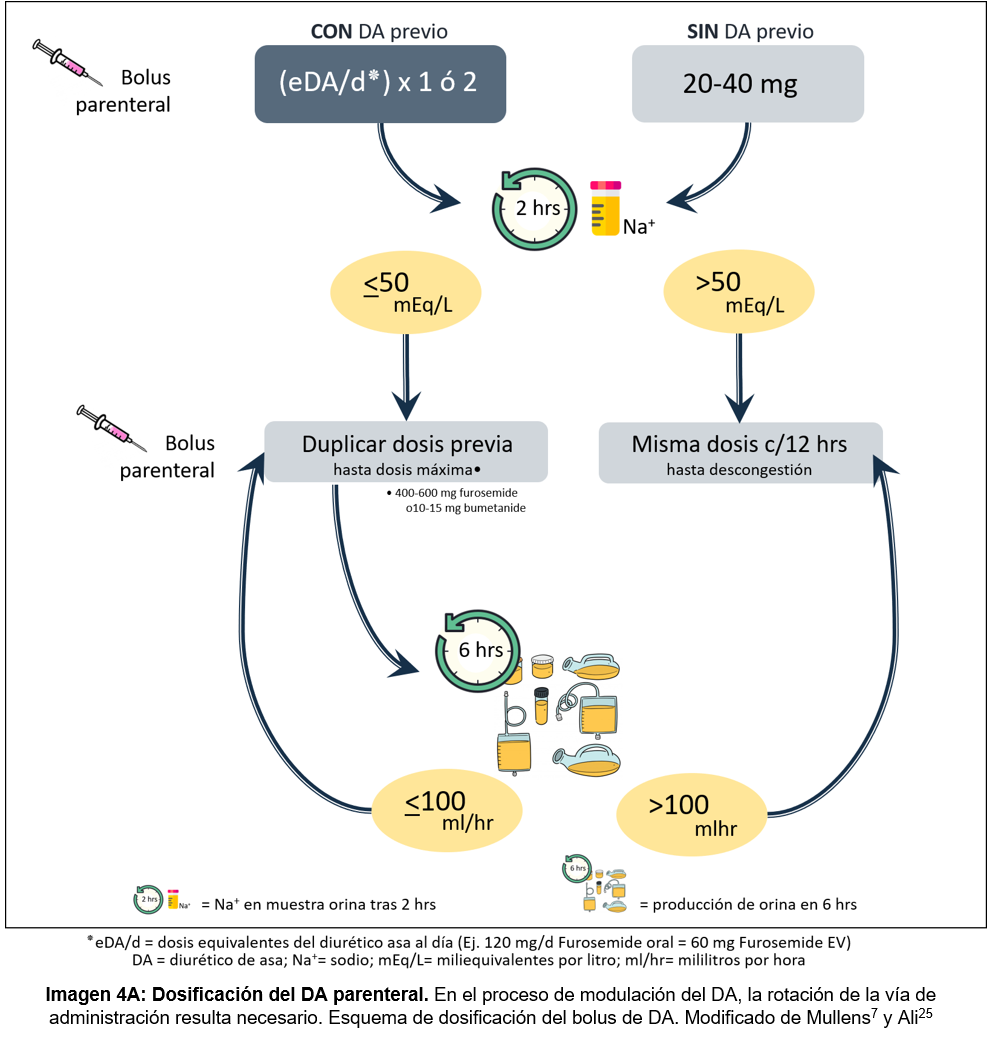
Aunque posiblemente útil en un inicio, los mecanismos compensadores antes mencionados (Tabla 1), limitarán eventualmente el efecto de la simple modulación del DA y condicionarán una pérdida de respuesta diurética.
La clave para evitar dicha pérdida reside en que de forma paralela a la fase de modulación se establezcan medidas específicas para contrarrestar los mecanismos compensadores.
El empleo conjunto de diuréticos con distintos mecanismos y sitios de acción es conocido como bloqueo secuencial de la nefrona y se ha asociado a una disminución en la RD.2 El grado de contribución y los mecanismos por los cuales los diuréticos permiten vencer la resistencia son variados y se encuentran resumidos en la Tabla 2.
Tabla 2: mecanismos de RD y estrategias para su tratamiento

Así, mientras se “acelera” en la dosificación del DA se deben introducir diversos fármacos con el objetivo de potenciar el efecto diurético y minimizar la RD (teniendo en cuenta los distintos mecanismos de resistencia, contraindicaciones de los diuréticos y las características del paciente) (figura 4).
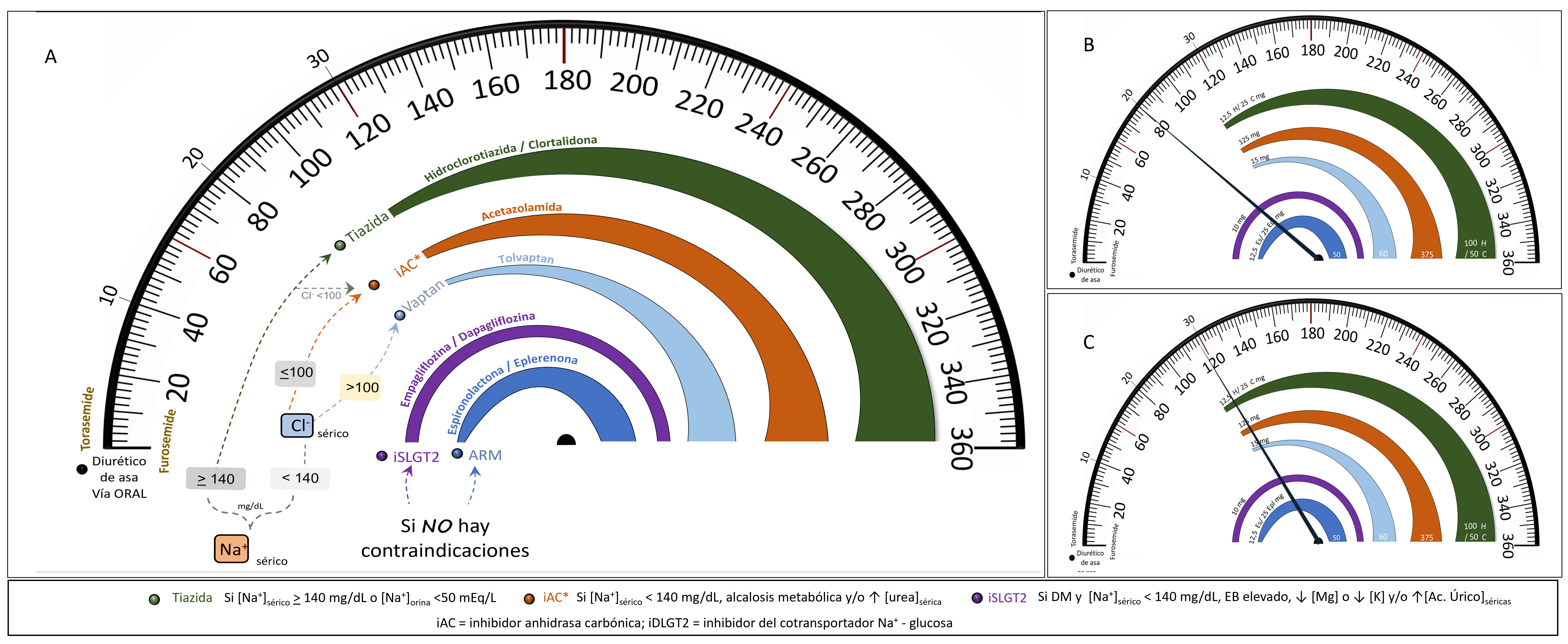
Imagen4: En la “carrera” de modulación de los diuréticos de asa, conforme “aceleramos” en la dosificación, otros fármacos deben de iniciarse para minimizar/contrarrestar los mecanismos compensadores. Por ejemplo, cuando se alcanzan dosis de 80 mg/día furosemide vía oral o su equivalente endovenoso (2:1) (figura b) se deben de estar administrando (si no hay contraindicación) un mínimo de 12,5/25 md/día de Aldactone/Eplerenona y 10 mg de un iSLGT2; pero al incrementar la dosis de furosemide a 120 mg/d (figura C), aparte de la titulación del diurético ahorrador de potasio, la incorporación de otros fármacos se hace indispensable. La elección de dichos fármacos dependerá de las características propias del paciente (ej, natremia, cloremia, estado ácido-base…) y contraindicación de los fármacos (ver tabla 2)
El empleo del Suero hipertónico (SHT) asociado a dosis elevadas de furosemide ha demostrado ser una importante herramienta20-22 contra la RD atenuando los efectos nocivos de la excitación neurohormonal propia de la IC avanzada, así como incrementando la presencia del diurético en su sitio de acción debido a que:
- El incremento del nivel plasmático de Cl– revierte el efecto de la hipocloremia en la retención de Na+.21
- El SHT osmóticamente atrae al espacio intravascular los líquidos promoviendo la diuresis sin depletar el intravascular.21
- El incremento del volumen intravascular previo a la diuresis reduce temporalmente la retención de Na+ mediada por estímulos neurohormonales.21
- Incremento en la contractilidad miocárdica.
Para su correcta dosificación se aconseja la administración de 100-150 cc de una solución hipertónica (de concentración variable en función de la natremia del paciente) en un tiempo aproximado de 30-60 minutos, de forma conjunta con dosis elevadas de furosemide (dosis recomendadas entre 125-250 mg, aunque se han descrito experiencias con infusión de hasta dosis de 1 gr de furosemide) y con un intervalo recomendado de 12 horas entre dosis (aunque intervalos mayores han sido descritos con adecuados resultados).20, 21
Distintas medidas encaminadas a mejorar la perfusión renal han sido empleadas con el objetivo de vencer la RD, aunque la falta de evidencia convincente las confina a situaciones muy limitadas en la práctica clínica diaria.2
Aunque la extracción de plasma isotónico presenta teóricas ventajas sobre el tratamiento deplectivo (al remover más sodio), el alto riesgo de complicaciones relacionadas al catéter, así como la ausencia de resultados significativos que avalen su empleo hacen que la ultrafiltración se considere como la última opción, en casos de refractariedad a todas las medidas anteriores.4-7
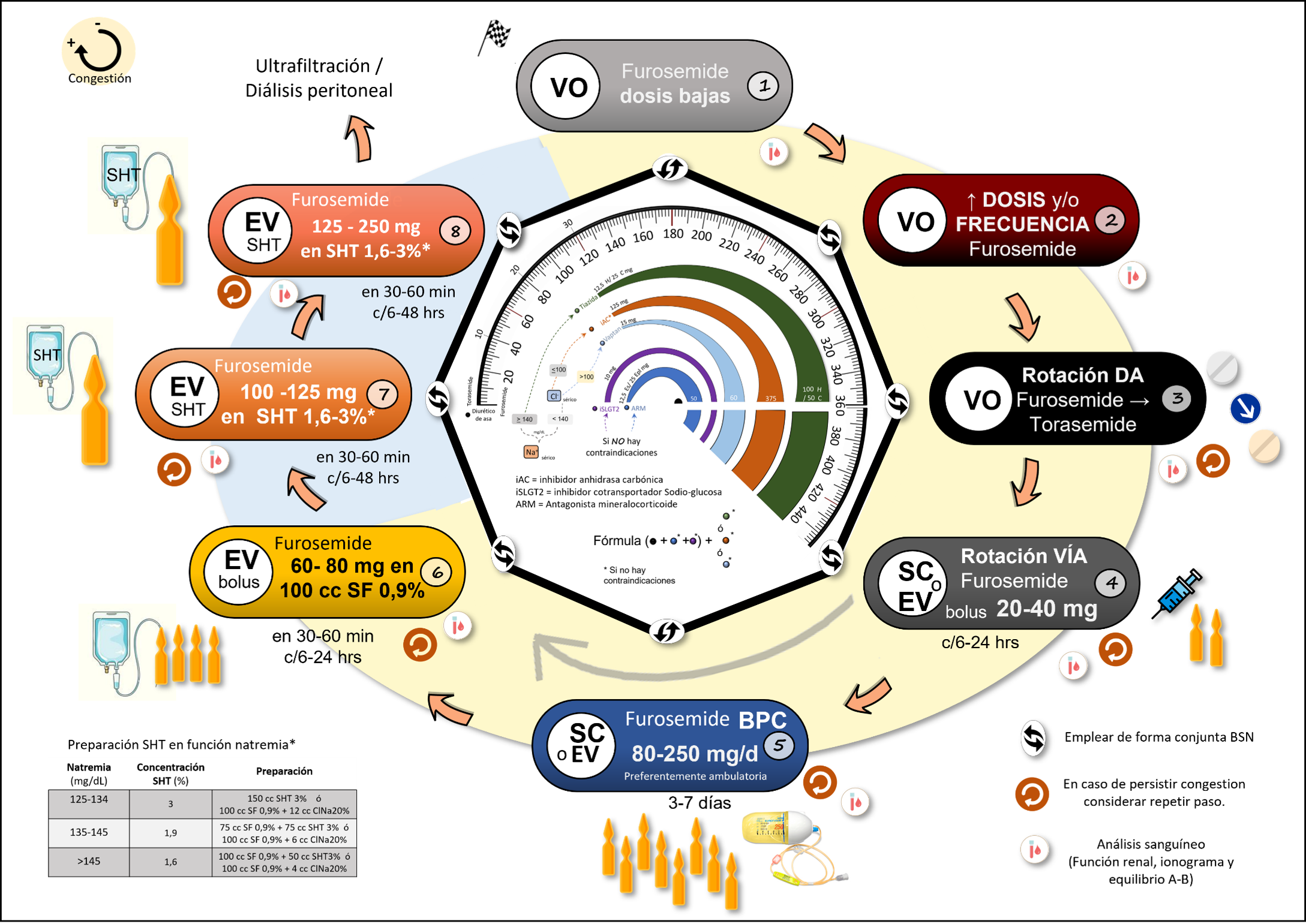
Esquema resumen de actuación ante la congestión: Conforme incrementa la congestión, de forma paralela a la modulación del DA, es determinante introducir y titular fármacos que permitan contrarrestar los mecanismos de RD. La elección de dichos fármacos dependerá de las características propias del paciente (ej. natremia, cloremia, estado acido-base..) y contraindicaciones de los fármacos. Adaptado de referencias 2-9,24,25
CONCLUSIONES:
La RD en la IC es frecuente, generalmente desapercibida, tratada en general muy tarde y en la mayoría de los casos de forma insuficiente condicionando hospitalizaciones, mal control de síntomas y muerte. Es por eso por lo que optamos por un tratamiento deplectivo coordinado que permita alcanzar la descongestión teniendo en cuenta los diversos mecanismos compensadores, y no basado en la simple titulación del diurético de asa, porque para vencer a la resistencia diurética debemos recordar ir más allá del asa.
iSLGT2 Diabetes Mellitus & enfermedad cardiovascular
En el siguiente enlace podéis ver una presentación de los iSLGT2 y de su utilidad en el abordaje terapéutico de la Diabetes Mellitus y de la Insuficiencia cardiaca
BIBLIOGRAFIA:
- Kristjánsdóttir, I. et.al. “Congestion and Diuretic in Acute or Worsening Heart Failure”. Card Fail Rev 2020 (6) 1-5.
- Felker, G. et.al “Diuretic Therapy for patients with heart failure” JACC 2020; 75(10):1178-95.
- Gupta, R. et.al. “Diuretic Resistance in Heart Failure” Curr Heart Fail Rep. 2019; 16(2):57-66
- Verbrugge, F. et.al. “Editor´s choice-diuretic resistance in acute heart failure” Eur Heart J 2018; 7(4):379-389
- Cox, Z. et.al. “Loop diuretic resistance complicating acute heart failure” Heart Fail Rev 2020; 25: 133-145
- Wilcox, C.S., et.al. “Pathophysiology of Diuretic Resistance and its implications for the management of Chronic Heart Failure”. Hypertension 2020; 76: 1045-1054
- Mullens W. et.al. “The use of diuretics in heart failure with congestion: a position statement from the Heart Failure Association of the European Society of Cardiology” Eur. J. Heart Fail 2019 (2);1-19.
- Hoorn, E. et.al. “Diuretic Resistance” Am J Kidney Dis. 2017 69 (1); 136-142
- Bowman, B. et.al. “Treating Diuretic Resistance” Cardiol Rev 2016; 24 (5): 256-260
- O´Connor CM, et.al. “Effect of nesiritide in patients with acute decompensated heart failure”. NEJM 2011; 365: 32-43
- Felker GM, et.al. “Efficacy and safety of tolvaptan in patients hospitalized with acute heart failure”. Am J Coll Cardiol 2017; 69: 1399-406.
- Konstam, MA et.al. “Short-term effects of tolvaptan in patients with acute heart failure and volumen overload”. J Am Coll Cardiol 2017; 69: 1409-19
- Verbrugge, F. et.al. “Acetazolamide to increase natriuresis in congestive heart failure at high risk for diuretic resistance”. Eur J Heart Fail 2019; 21: 1415-1422
- Kataoka, H. et.al. “Treatment of Hyponatremia with Acetazolamide in Cardiovascular patients: Possible alternative diuretic to vasopressin antagonist” Ann Cardiol Vasc Med 2020: 3(1);1032-39
- Kataoka, H. et.al. “Treatment of hypochloremia with acetazolamide in an advanced heart failure patient and importance of monitoring urinary electrolytes”. J. Cardiol 2018;17: 80-84.
- Greval, G. et.al. “Feasibility study to determine if administration of carbonic anhydrase inhibidor Acetazolamide will cause aquaresis but prevent hiponatremia in a healthy population: SALT study”. J Integ Cardiol 2018; 4(4):1-3
- Mullens, W. et.al. “Rationale and design of the ADVOR (Acetazolamide in decompensated heart failure with volumen overload) trial” Europ J Heart Fail. 2018 (11):1591-1600
- Mordi, N. et.al “Renal and Cardiovascular effect of SLGT2 inhibition in combination with loop diuretics in patients with type 2 diabetes and chronic heart failure”. Circulation. 2020; 142: 1713-24.
- Kimura, G. et.al. “Diuretic action of sodium-glucose cotransporter 2 inhibitors and its importance in the management of heart failure”. Circul J. 2016; 80: 2277-2281.
- Griffin, M. et.al. “Real world use of hypertonic saline in refractory acute decompensated heart failure”. JACC 2020; 8:199-208.
- Covic, A. et.a. “Efficiency of Hypertonic saline in the management of decompensated heart failure: A systematic review and meta-analysis of clinical studies” Am J Cardiovasc Drugs. 2020;6: 559-570.
- Costanzo, MR. “Hypertonic Saline” JACC 2020 8; 1-3
- Sharma, K. et.al. “Randomized evaluation of heart failure with preserved ejection fraction patients with acute heart failure and dopamine: the ROPA-DOP trial”. JACC Heart Fail. 2018; 6:859-870.
- Nuñez J, Báyes-Génis A. et.al. Congestión en IC [Internet].2020 [citado 10 noviembre 2020]. Disponible en: https://www.svcardio.org/congestionguilty
- Ali, S . et.al. “Inpatient diuretic management of acute heart failure: a practical Review”. Am J Cardiovasc Drug 2021 EPUB 10.1007/s40256-020-00463-5